在当前“医药创新”的时代浪潮下,越来越多传统药企在开发仿制药的同时,开始加码创新药研发。其中,齐鲁制药以仿制药为基,创新药为抓手,同时大力开展出海,除今年新上市小分子化学1类创新药伊鲁阿克片(NSCLC重磅药)外,还有35款1类新药在研。
伊鲁阿克片是国内第二款获批的国产ALK,也是齐鲁制药首个1类创新药,于今年6月28日获国家药品监管局批准上市,对于齐鲁制药来说具有里程碑意义。该药不仅可抑制不同融合类型的野生型以及ALK耐药突变的ALK激酶活性,同时还可有效抑制不同融合类型ROS1激酶的活性。适用于既往接受过克唑替尼治疗后疾病进展或对克唑替尼不耐受的间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者,今年4月第2项适应症(治疗ROS1阳性非小细胞肺癌)提交上市申请。
肺癌发病率及死亡率均居所有恶性肿瘤之首,据WHO统计,全球每年新增肺癌患者120万。据WHO国际癌症研究机构数据,2020年我国新发肺癌病例数约为82万;国家癌症中心数据,我国的肺癌发病数和死亡数分别占全球的37%和39.8%,远高于我国占世界人口18%的比例。这些肺癌患者中,80%以上为非小细胞型肺癌(NSCLC),约75%在发现时已处于中晚期。
ALK因其靶向药物治疗效果良好,是晚期NSCLC的重要治疗靶点之一,再因市场需求旺盛,十余年来全球多家企业布局该靶点,已迭代至四代。海外布局企业有辉瑞、阿斯利康、诺华等;本土布局企业有齐鲁制药、贝达药业、正大天晴、再鼎医药等,其药物已获批上市或申请上市。轩竹生物、上海药物研究所、塔吉瑞生物、泽璟制药等的临床研究处于2期或以上,另有首药控股的CT-707、北京浦润奥生物的PLB1003等处于临床1期阶段。
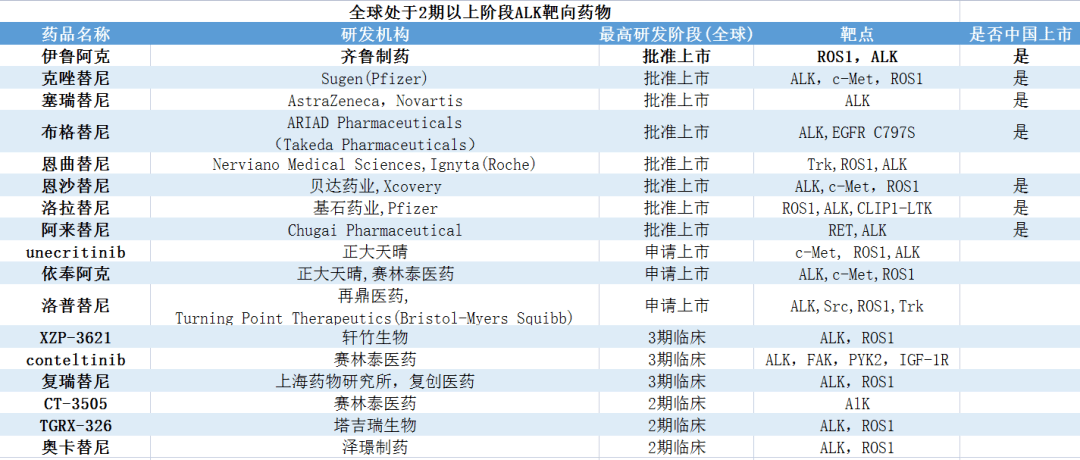
中国非小细胞肺癌靶向药市场到2025年或将突破1000亿元。目前除几款进口药品上市外,中国本土自主开发的ALK仅有贝达药业的恩沙替尼(2020年11月)、齐鲁制药的伊鲁阿克(2023年6月)获批上市。
目前国内ALK主要由海外巨头辉瑞的克唑替尼、罗氏的阿来替尼占据主要市场。贝达药业的恩沙替尼本土首发,率先向进口药挑战,推进国产替代。公开资料显示,贝达药业的恩沙替尼2021年实现收入约1.5亿元,2022年实现快速放量,同比增长高达684.32%,达5.4亿元。2023年上半年恩沙替尼销量同比增长12.02%。今年6月齐鲁制药的伊鲁阿克片获批上市,贝达药业恩沙替尼的先发优势将会减退,二者将一较高下。此外随着未来本土多款ALK上市,市场竞争将拉至高点。
除了伊鲁阿克片进军肺癌赛道,齐鲁制药另有注射用培美曲塞二钠在2006年就布局该赛道。该药2006年在中国上市,2011年首家获准用于非鳞状非小细胞肺癌的一线年获FDA批准上市,还在西班牙、丹麦、瑞典等欧盟国及英国获批上市。
注射用培美曲塞二钠原研厂家是礼来,国内首仿资格由江苏豪森在2005年获得。目前国内市场由四川汇宇制药、齐鲁制药、礼来、江苏豪森、扬子江药业、江苏奥赛康药业、先声药业、苏州二叶制药等20余家药企共同瓜分。综合米内网及药融云数据库数据,该药2021年销售额超过44亿元,2022年受集采影响下滑24.93%,仅剩28.59亿元。2022年,四川汇宇制药占市场份额43.69%,礼来16.42%、豪森药业14.35%、齐鲁制药11.97%。
齐鲁制药另有国内首仿NSCLC一线靶向特效药物吉非替尼片,以不到进口药三分之一之价格,打破阿斯利康原研药在中国的市场垄断地位,并出海英国、德国、西班牙、美国等。目前本土吉非替尼由阿斯利康、齐鲁制药和正大天晴组成三足鼎立之势。2022年,吉非替尼国内销售6.64亿元,三甲市占率分别为:阿斯利康54.59%、齐鲁制药25.43%、正大天晴17.60%。另外上海创诺制药、恒瑞医药、湖南科伦制药、扬子江药业、江苏天士力帝益药业等均占据一定市场份额。
除了布局恶性肿瘤之首的肺癌赛道,齐鲁制药还深入全球发病率第二高的乳腺癌领域,如国内首个CDK4/6仿制药哌柏西利。
CDK4/6相比较HER2靶向药物,可有效克服或延迟内分泌抵抗的出现,为患者争取更长的生存时间,是乳腺癌靶向药新贵。据WHO数据,目前全球每年新增乳腺癌患者约100万。在中国,乳腺癌发病率位居女性恶性肿瘤之首。2020年全球CDK4/6市场规模达69.92亿美元。
目前,全球共有5款CDK4/6上市,分别是:辉瑞的哌柏西利、诺华的瑞波西利、礼来的阿贝西利、恒瑞医药的达尔西利、BI/先声药业的曲拉西利。上述5款CDK4/6全部在中国上市。本土布局CDK4/6的企业有近20家,如:复星医药(子公司锦州奥鸿药业的FCN-437c胶囊,上市申请于今年11月21日获NMPA受理)、四环医药(附属公司轩竹生物的吡罗西尼,上市申请于今年9月5日获NMPA受理);另有翰森制药、甘李药业、倍尔达、正大天晴进入2期临床试验,贝达药业、基石药业、晟科药业、勋和医药、必贝特医药等进入1期临床试验。
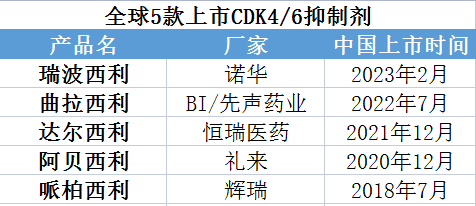
哌柏西利原研厂家是辉瑞,是全球首个上市的细胞周期蛋白依赖性激酶(CDK)4/6,2015年美国上市,2018年中国上市,曾占据全球CDK4/6市场份额超77%。据辉瑞年报,2020年至2022年三年间,哌柏西利的销售额均稳定在50亿美元以上。今年1月,哌柏西利中国化合物专利到期,包含齐鲁制药的本土多家企业开展仿制。据丁香园Insight数据库,齐鲁制药早在2015年便开展了哌柏西利仿制药的临床试验,2020年11月获批上市,是国内首个哌柏西利仿制药,以其明确的疗效打破了乳腺癌原有治疗局限。
据药融云数据,目前,除了齐鲁制药(国内首仿),国内还有多家药企的哌柏西利胶囊仿制药获批上市:江苏豪森药业(翰森制药附属公司)、江西山香药业(青峰医药子公司)、江苏奥赛康和四川科伦药物研究院有限公司(科伦药业子公司)等。哌柏西利片剂仿制药方面,齐鲁制药、石药集团、南京正大天晴等均已提交上市申请。另外还有重庆药友、上海创诺、北京泰德、先声药业等提交仿制药上市申请。可以预见,未来,围绕进口与国产、仿制与原研、胶囊与片剂的哌柏西利厮杀将火热至极。
此外,齐鲁制药另有一款药物布局乳腺癌及肺癌赛道——多西他赛注射液(2003年上市)。该药在临床上主要用于先期化疗失败的晚期或转移性乳腺癌的治疗,以及以顺铂为主的化疗失败的晚期或转移性非小细胞肺癌的治疗。
多西他赛原研厂家是赛诺菲,在我国上市以后,院内销售额最高达36亿元,销售量最高达到803万。恒瑞医药、正大天晴、扬子江药业、齐鲁制药、汇宇制药、奥赛康药业均布局该药物,且共同参与了第五批集采。随后的2022年,多西他赛全市场销售额大跌73%,仅剩6亿元,赛诺菲来到市场第一(市场占比35.34%)、恒瑞第二,齐鲁制药等占据一定市场份额。另外布局企业还有瀚晖制药、上海上药、太极集团、辰欣药业等共计超20家。
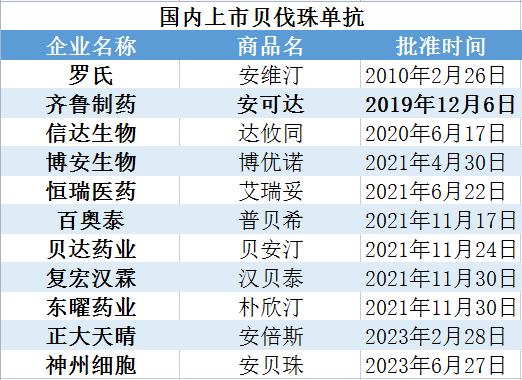
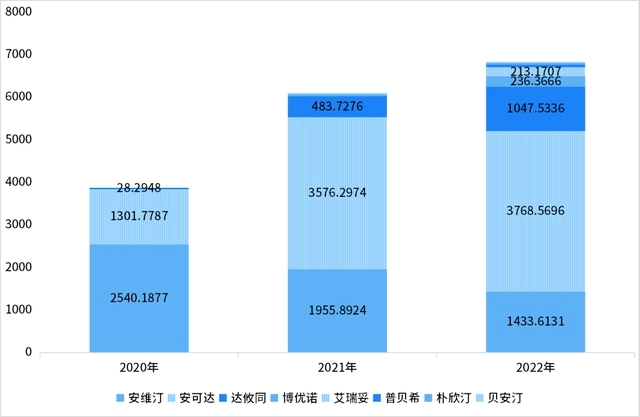
贝伐珠单抗是抗肿瘤药物的王牌,原研厂家是罗氏,其在中国的专利保护在2018年到期。齐鲁制药的贝伐珠单抗生物类似药(安可达)2019年12月在国内上市,为国内首家。目前国内贝伐珠单抗初步形成“1家原研+10家仿制”格局。齐鲁制药的安可达由于价格等优势在2021年便远超原研厂家罗氏。2022年,贝伐珠单抗中国本土销售达65亿元,其中齐鲁制药样本医院销售额约38亿元,占比54.74%,位居国内市场第一;罗氏(14.87亿元,占比22.89%)列第二;信达生物(11.13亿元,占比17.13%)位列第三。贝伐珠单抗的中国市场规模将高达百亿元,目前,含上述药企在内,本土共有近20家药企均布局了该赛道,未来竞争将会非常激烈。
齐鲁制药还有G-CSF升白药新瑞白,长期占据国内主要市场。G-CSF分短效和长效两种,国内市场达百亿元。短效方面,2022年齐鲁制药占据最大市场份额,销售额7.29亿元,市占率32.54%;特宝生物(市占率9.34%)、九源基因(市占率8.98%)和双鹭药业(市占率8.40%)分列其后。长效方面主要由三家企业占据市场,2022年,石药百克销售额25.99亿元(市占率40.12%);齐鲁制药销售额22.78亿元(市占率35.16%);恒瑞医药销售额15.53亿元(市占率23.96%)。另外,科兴生物、江苏奥赛康、天津派格生物、深圳未名新鹏生物、重庆富进生物、中美福源等均进入该赛道。即便未来或面临集采,但本土药企称霸的G-CSF赛道竞争将持续。
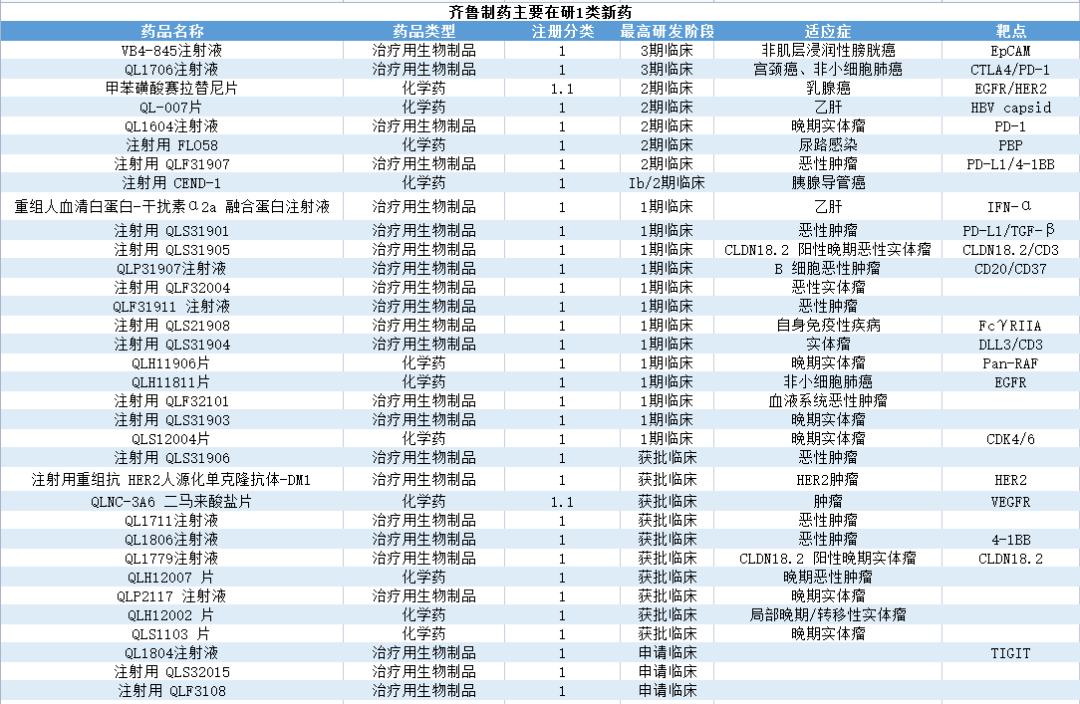
此外,今年以来,齐鲁制药还有奥拉帕利片(国内首仿)、培唑帕尼片(国内首仿)、溴莫尼定噻吗洛尔滴眼液(单剂量包装为国内独家上市)、恩扎卢胺软胶囊、盐酸尼洛替尼胶囊等多款产品上市。另有35个1类新药处于申报临床及以上阶段。
2020年,齐鲁制药实现销售收入275亿元,2021年344亿元,2022年375亿元,销售额连年攀升。不过从上文也可看出,虽然齐鲁制药拥有多款重磅药物,但药物所在赛道竞争均激烈,这或许也是齐鲁制药大力加码创新药研发的原因——以生物类似药为基、大力开展创新药研发,占取更多市场。
此外持续对标欧美实现出海,长期合作伙伴有默克、辉瑞、诺华等国际制药巨头,并同时向欧、美、英、日、澳、加法规市场出口制剂,有超40个产品在全球或所销国市占率第一。2022年,齐鲁制药出口额达9.2亿美元,同比逆势增长21%。
3.《非小细胞肺癌靶向治疗!国内上市的6款ALK疗效如何?》,药融云,2022-12-08.
4.《国产之光!齐鲁新一代ALK伊鲁阿克获NMPA批准上市》,凯莱英药闻, 2023-06-30.返回搜狐,查看更多